3 maneiras incríveis pelas quais os químicos sintetizaram compostos este ano
Por Bethany Halford
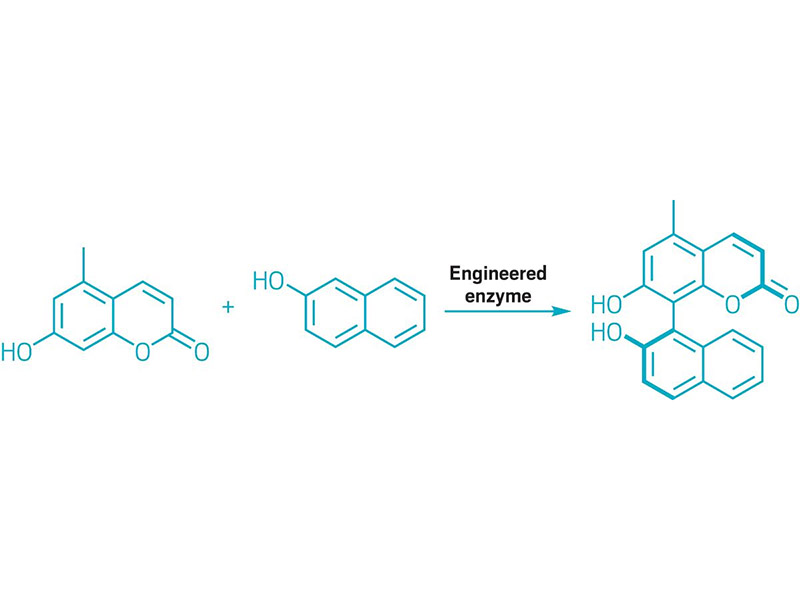
ENZIMAS EVOLUÍDAS CONSTRUÍRAM LIGAÇÕES BIARÍLICAS
Esquema ilustrando um acoplamento biarílico catalisado por enzima.
Químicos utilizam moléculas biarílicas, que apresentam grupos arila ligados entre si por uma ligação simples, como ligantes quirais, blocos de construção de materiais e produtos farmacêuticos. No entanto, a síntese do motivo biarílico por meio de reações catalisadas por metais, como os acoplamentos cruzados de Suzuki e Negishi, geralmente requer várias etapas sintéticas para a obtenção dos parceiros de acoplamento. Além disso, essas reações catalisadas por metais apresentam dificuldades na síntese de biarilas volumosas. Inspirada pela capacidade das enzimas de catalisar reações, uma equipe liderada por Alison RH Narayan, da Universidade de Michigan, utilizou evolução dirigida para criar uma enzima citocromo P450 capaz de sintetizar uma molécula biarílica por meio do acoplamento oxidativo de ligações carbono-hidrogênio aromáticas. A enzima une moléculas aromáticas para criar um estereoisômero em torno de uma ligação com rotação impedida (ilustrada na figura). Os pesquisadores acreditam que essa abordagem biocatalítica pode se tornar uma transformação fundamental para a produção de ligações biarílicas (Nature 2022, DOI: 10.1038/s41586-021-04365-7).

A receita para aminas terciárias dependia de um pouco de sal.
O esquema mostra uma reação que produz aminas terciárias a partir de aminas secundárias.
A mistura de catalisadores metálicos ávidos por elétrons com aminas ricas em elétrons geralmente destrói os catalisadores, portanto, reagentes metálicos não podem ser usados para construir aminas terciárias a partir de aminas secundárias. M. Christina White e seus colegas da Universidade de Illinois em Urbana-Champaign perceberam que poderiam contornar esse problema adicionando um elemento salino à sua receita de reagentes. Ao transformar aminas secundárias em sais de amônio, os químicos descobriram que podiam reagir esses compostos com olefinas terminais, um oxidante e um catalisador de sulfóxido de paládio para criar inúmeras aminas terciárias com uma variedade de grupos funcionais (exemplo mostrado). Os químicos usaram a reação para produzir os medicamentos antipsicóticos Abilify e Semap e para transformar medicamentos existentes que são aminas secundárias, como o antidepressivo Prozac, em aminas terciárias, demonstrando como os químicos podem criar novos medicamentos a partir de medicamentos já existentes (Science 2022, DOI: 10.1126/science.abn8382).
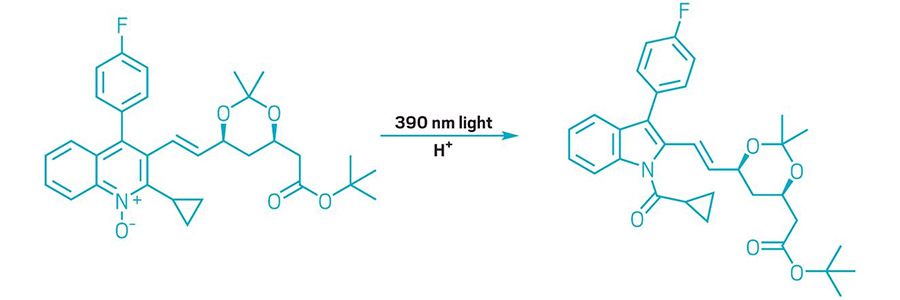
AZAARENOS SOFRERAM CONTRAÇÃO DE CARBONO
O esquema mostra um N-óxido de quinolina transformado em um N-acilindol.
Este ano, químicos ampliaram o repertório de edição molecular, que consiste em reações que modificam os núcleos de moléculas complexas. Em um exemplo, pesquisadores desenvolveram uma transformação que utiliza luz e ácido para remover um único carbono de azaarenos de seis membros em N-óxidos de quinolina, formando N-acilindóis com anéis de cinco membros (exemplo mostrado). A reação, desenvolvida por químicos do grupo de Mark D. Levin na Universidade de Chicago, é baseada em uma reação que envolvia uma lâmpada de mercúrio, a qual emite luz em múltiplos comprimentos de onda. Levin e seus colegas descobriram que o uso de um diodo emissor de luz (LED) que emite luz a 390 nm proporcionava um controle mais preciso e permitia generalizar a reação para N-óxidos de quinolina. A nova reação oferece aos sintetizadores de moléculas uma maneira de remodelar os núcleos de compostos complexos e pode auxiliar químicos medicinais que buscam expandir seus bancos de candidatos a fármacos (Science 2022, DOI: 10.1126/science.abo4282).
Data da publicação: 19/12/2022

